Сандлер Б.И., Чудновский В.М., Юсупов В.И., Галин Ю.М. Лечение компрессионных и рефлекторных синдромов поясничного остеохондроза методом ППЛДД.
Институт медицинской физики им. У.Х. Копвиллема
Приморский краевой диагностический центр, г. Владивосток
УДК: 616.721.6-018.3-06.616.833.24-008.6-89.168
Остеохондроз позвоночника, тесно связанный как дегенеративно-дистрофический процесс с процессами старения организма, относится к наиболее распространенным заболеваниям человека. В амбулаторно-поликлинических учреждениях больные с дискогенными болевыми синдромами среди других неврологических больных составляют до 70 %, а в стационарных 55,5 % [1]. При этом удельный вес поражений поясничного отдела позвоночника составляет 60-90 % [2]. Хронический рецидивирующий характер течения, прогрессирующий рост заболеваемости и высокий процент инвалидности среди лиц трудоспособного возраста придает данной проблеме особую социальную значимость. Консервативное лечение, назначаемое при данной патологии более чем в 90 % случаев, как правило, имеет положительный, но временный эффект и нередко затягивается на годы, что также приводит к социальной дезадаптации больного, а часто и к инвалидности [3]. Современная классификация заболеваний периферической нервной системы [2] включает в клиническую вертебрологию синдромы, возникающие вследствие поражений позвоночника, разделяя их на компрессионные и рефлекторные (мышечно-тонические и нейротрофические). А.И. Осна [10] и Я.Ю. Попелянский [11], относят сюда также нейровисцеральные проявления, а нейротрофические изменения определенных зон опорно-двигательного аппарата, развившиеся вследствие импульсации из пораженного позвоночного двигательного сегмента определяют как нейроостеофиброз.
В настоящее время выделяют четыре основных механизма для формирования вертеброгенных синдромов при остеохондрозе позвоночника: компрессионный, дисфиксационный, дисгемический и асептико-воспалительный.
Однако следует подчеркнуть, что клиническую картину заболевания определяет совокупность данных патогенетических факторов при ведущей роли, как правило, одного из них.
Нашей задачей является, в основном, рассмотрение некоторых аспектов хирургического лечения компрессионных форм поясничного остеохондроза.
Применявшаяся ранее повсеместно с целью хирургического лечения грыж межпозвонковых дисков открытая спинальная дискэктомия посредством ляминэктомии была самым удобным способом для ревизии корешков и удаления грыжевого выпячивания, но имела многочисленные недостатки, связанные с травматизацией тканей определенного позвоночного сегмента. Вследствие этого в оперированном сегменте позвоночника развивались нарушения в виде нестабильности, фиброза мышц с последующим дефицитом функций мышц спины, послеоперационного арахноидита и стеноза позвоночного канала из-за развития эпидурального рубца. Все эти факторы приводили вновь к болям в спине и рецидиву корешкового синдрома, а при анализе результатов операций в отдаленном периоде выявлялось от 28 до 53 % неудовлетворительных исходов [6, 7, 8, 13, 14, 16, 18, 20].
Более ограниченные по объему виды заднего доступа: такие как гемиляминэктомия, фораминотомия, интерламинэктомия, трансверсо-артропедикулоэктомия не гарантируют от тех же осложнений, хотя и менее выраженных [4, 18].
В дальнейшем тенденция к уменьшению объема оперативного вмешательства при лечении дискогенного корешкового синдрома выразилась в трех направлениях: хемонуклеолиз, микрохирургическая дискэктомия и чрезкожная дискэктомия.
Микродискэктомия, хотя и позволяет щадящим путем удалить измененные и секвестрирующиеся участки межпозвонкового диска и избежать грубых дистрофических и некротических изменений в тканях диска, однако также является открытым оперативным вмешательством и поэтому несвободна от вышеуказанных неблагоприятных последствий открытой операции: травматизации мягких тканей, хотя и в меньшем объеме, резекции краев дужек позвонков, травмы сосудов и др. анатомических образований за границами диска, развития эпидурального рубца [8, 15, 23, 32, 34].
В 1963 г. L . Smith ввел в практику хемонуклеолиз, который получил широкое распространение как нашей стране, так и за рубежом [3, 4, 22, 29]. Однако, стабилизация позвоночника, необходимая для достижения хорошего результата, увеличивает время лечения [3].
Затем был разработан метод эндоскопической нуклеотомии, автоматизированной отсасывающей нуклеотомии и чрезкожной механической нуклеэктомии, когда не вскрывается позвоночный канал, не нарушается стабильность позвоночника и мало травмируются ткани по ходу операционного воздействия. При этом применение перечисленных методов было ограничено значительным количеством противопоказаний [21, 33, 35, 37].
В дальнейшем, появление высокоэнергетических лазерных аппаратов, передающих лазерную энергию по тонким световодам, позволило перейти в хирургическом лечении протрузий и грыж межпозвонковых дисков на качественно новый уровень: появился метод перкутанной лазерной дискэктомии и декомпрессии поясничных дисков [24, 26, 27, 31, 36].
Авторы, использующие лазерное излучение для чрезкожной декомпрессии дисков, отмечают положительные результаты лечения от 54 до 95 % [19, 24, 30, 31]. Однако отмечают до 10 % осложнений в виде кратковременной корешковой дизестезии, симпатических медиаторных болей или симпатодистрофий и единичных гематом поясничной мышцы.
Материал и метод
Для лечения больных поясничным остеохондрозом на основе использования полупроводникового лазера нового поколения типа «Лазон-10-П» нами разработан метод пункционной поликанальной лазерной декомпрессии диска (ППЛДД), являющийся усовершенствованным вариантом неэндоскопической лазерной декомпрессии межпозвонковых дисков и лазерной нуклеотомии.
Метод основывается на воздействии излучения полупроводникового лазера «Лазон-10-П» с длиной волны 960 нм на ткань межпозвонкового диска. Воздействие лазерного излучения с применением методики ППЛДД приводит к формированию в пораженном диске нескольких полостей общим объемом около 2-3 см 3 . А поскольку даже малое изменение в объеме диска связано с большими изменениями давления [9, 25], то уменьшение внутридискового давления меняет градиент между студенистым ядром и тканью, окружающей грыжевое выпячивание, в результате грыжа заталкивается обратно в диск.
Выполняя данную лазерную операцию, мы стремились к миниатюризации хирургического инструмента и лазерных световодов, что позволяет рассматривать эту процедуру как микрохирургическую. Операция выполнялась под местной анестезией с потенцированием. Пациента укладывали на стол в рентгеноперационной на левый бок. Манипуляция осуществлялась под контролем электронно-оптического преобразователя (ЭОП).
В случае протрузии диска L 4- L 5 пункцию производили из модифицированного бокового доступа Де Сез и Левернье. Диск L 5- S 1 пунктировали по способу, предложенному Эрлахером, что обеспечивало доступ к заднебоковым и центральным отделам диска. При этом вначале диск пунктировали проводником диаметром 0,5 мм, который после перфорации фиброзного кольца продвигали до третьей четверти диска. Особое внимание уделяли расположению иглы параллельно замыкательным пластинкам позвонков. Положение проводника и иглы контролировали ЭОП в двух плоскостях. Поскольку игла, введенная через проводник, располагалась по отношению к горизонтальной линии под углом 35-40 ° , трубку ЭОП ориентировали перпендикулярно ходу иглы. При пункции диска часто отмечался «провокационный тест»: усиление болевого синдрома с иррадиацией в ногу. Далее в иглу вводили световод диаметром 300 мкм, подключенный к лазерной установке «Лазон-10-П», на которой устанавливали мощность 3 Вт. Энергетическое воздействие через прямую иглу осуществлялось от 1 до 1,5 минут. Затем через тот же прокол заводили изогнутую специальным образом иглу, позволяющую подводить лазерную энергию как можно ближе к грыжевому выпячиванию. Общее энергетическое воздействие на диск зависело от величины грыжевого выпячивания, высоты межпозвонкового промежутка и составляло от 360 до 720 Дж.
В послеоперационном периоде больным назначали в течение 5 дней антибиотики и, по показаниям, нестероидные противовоспалительные препараты. Больные вставали на следующий день, садиться им разрешалось через 5-7 дней. Восстановительное лечение у подавляющего большинства больных проводилось амбулаторно.
На рисунке 1 схематично представлено формирование двух цилиндрических полостей в задних и центральных отделах межпозвонкового диска из одного пункционного доступа. Под контролем флюороскопии мы стремились к тому, чтобы эти каналы проходили как можно ближе к месту локализации грыжевого выпячивания. После осуществления пункционной поликанальной лазерной декомпрессии диска запускается процесс, приводящий к уменьшению плотности и размеров грыжевого выпячивания вплоть до его полного рассасывания.
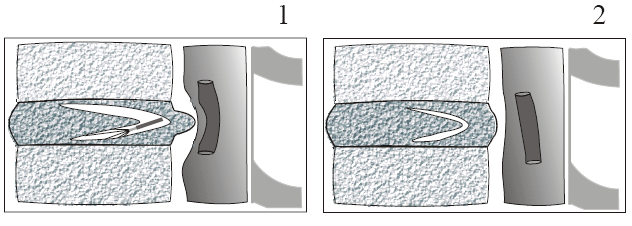 |
| Рис. 1. Схематичное представление формирования двух каналов в межпозвонковом диске: 1 – во время лазерной операции, 2 — спустя некоторое время после ППЛДД |
Схематично этапы этого процесса представлены на компьютерной модели (рис. 2). Здесь изображен поперечный разрез межпозвонкового диска с грыжевым выпячиванием. Стрелки показывают силы, действующие на контур диска изнутри и снаружи. В зависимости от положения тела давление внутри диска составляет от 50 до 200 кПа. Во время выполнения лазерной декомпрессии формируется полость 2-3 см 3 . При этом появляются равнодействующие силы, действующие на грыжевое выпячивание, направленные вовнутрь диска.
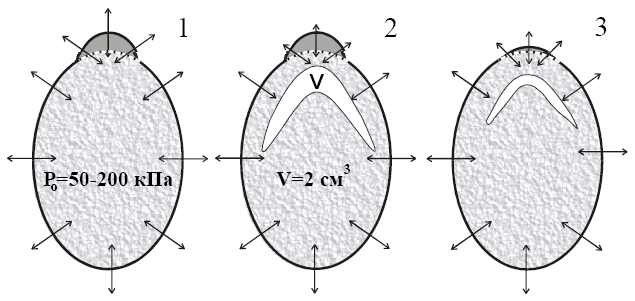 |
| Рис. 2. Компьютерная модель ППЛДД. Стрелки показывают силы, действующие на контур диска: 1 – до операции, 2 – сразу после операции, 3 – спустя некоторое время после ППЛДД. |
Представлены результаты лечения 115 больных с рефлекторно-болевыми и компенсированными синдромами поясничного остеохондроза методом ППЛДД со сроками послеоперационного наблюдения от трех месяцев до двух лет. Среди них были 41 женщина и 74 мужчины в возрасте от 15 до 71 года.
Почти всем этим больным неоднократно проводилось консервативное лечение в амбулаторных и стационарных условиях с применением комплекса медикаментозной терапии, физиотерапии, массажа, лечебной гимнастики, мануальных воздействий, иглорефлексотерапии. Консервативное лечение давало временный эффект. Больные были направлены к хирургу обычно в связи с затянувшимся обострением (4-6 мес.) и малой эффективностью традиционных методов лечения.
При клиническом обследовании у пациентов были выявлены признаки дегенеративного поражения позвоночника: сглаженность поясничного лордоза, напряжение паравертебральных мышц и другие мышечно-тонические синдромы, такие как синдром грушевидной мышцы, средней и малой ягодичных мышц, приводящих и задних мышц бедра, а также проявления нейродистрофического синдрома крестцово-подвздошного сочленения. У многих больных наблюдался анталгический наклон туловища в виде кифосколиоза. В неврологическом статусе отмечались симптомы натяжения нервных стволов, а также признаки раздражения и компрессии нервных корешков вплоть до клинических проявлений радикулоишемии с парезами мышц нижних конечностей в дистальных отделах.
Основные клинические проявления поясничного остеохондроза у наших пациентов представлены в таблице 1. Нозологическое распределение болевых синдромов представлено в таблице 2.
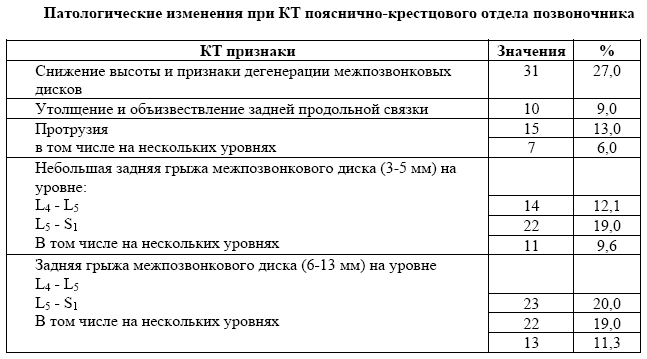
На догоспитальном этапе почти всем пациентам была проведена компьютерная или магнитно-резонансная томография. Обнаруженные патологические изменения при КТ пояснично-крестцового отдела позвоночника представлены в таблице 3. Во всех случаях обнаружена протрузия или грыжа диска на уровне L 4 — L 5 или L 5 — S 1 различной степени выраженности, что и было расценено как одна из возможных причин болевого синдрома. При этом грыжи диска средних и больших размеров (6-13 мм) в наших наблюдениях преобладали над небольшими грыжами дисков (3-5 мм): их число составляло соответственно 45 и 36.
Таблица 1
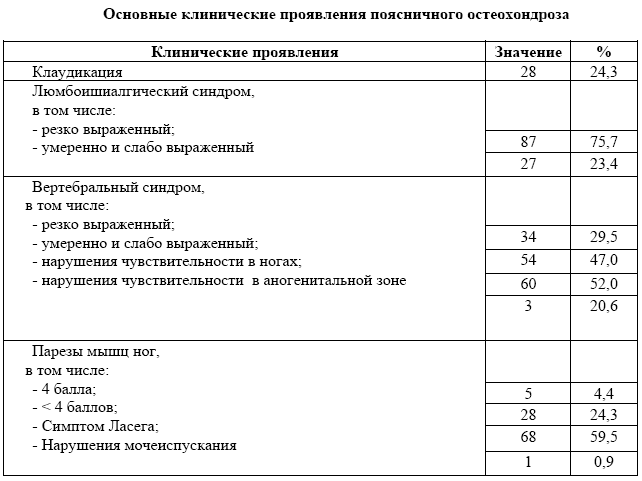
Таблица 2

Таблица 3
Показаниями для хирургического лечения представленных больных методом неэндоскопической лазерной декомпрессии диска в виде ППЛДД являлись боли в поясничной области типа люмбалгии или люмбаго хронического характера, люмбоишиалгические и корешковые синдромы, а также мышечно-тонические болевые синдромы и радикулоишемии дискогенного происхождения.
В большинстве наблюдений уже на операционном столе или на следующий день отмечался регресс неврологической симптоматики: болевого синдрома, симптомов натяжения нервных стволов, корешкового синдрома. Наблюдалось уменьшение или исчезновение нарушений кожной чувствительности.
Синдром радикулоишемии пятого поясничного или первого крестцового корешка с нарушением активных движений в стопе наблюдался у 33 больных. Только у трех из них не было эффекта от лечения из-за давности неврологического дефицита более года.
У остальных уже в первые часы после операции наступило восстановление активных движений в стопе в полном объеме с мышечной силой до 4 или 5 баллов.
Восстановление статики — биомеханики позвоночника происходило более медленно. Однако у всех больных в разные сроки отмечался полный регресс анталгических наклонов туловища даже при выраженности исходного кифосколиоза более 70-80 ° . Поэтому дискомфортный синдром в позвоночнике сохранялся до нескольких недель, оставаясь в слабом виде у некоторых больных в виде резидуальных болей. Сроки наблюдения в послеоперационном периоде составили от 3 мес. до 2 лет. Через три месяца после операции и через год некоторым больным проведено контрольное компьютерное томографическое исследование позвоночника. Из 50 таких исследований через 3 мес. после операции в 40 %
случаев отмечалось полное или почти полное рассасывание грыжевого выпячивания, в 33 % наблюдений грыжа диска уменьшалась в объеме до 50 % от первоначальной величины, измеряемой при мультипланарной реконструкции в сагиттальной плоскости. В остальных 27 % случаев наблюдалось изменение контуров грыжевого выпячивания. Таким образом, на контрольных компьютерных томограммах компрессия нервных корешков и дурального мешка не определялась или стала незначительной и клинически не проявлялась. Следует отметить, что при исследовании через год после операции отмечалась тенденция, хотя и на небольшом количестве наблюдений (20) к увеличению числа случаев полной деградации грыжевых выпячиваний до 60-70 %.
Оценка результатов лечения проводилась с помощью шкалы классификации боли от 0-0 (полное отсутствие боли) до 10 — сильная боль [28].
Учитывалась также степень возвращения к активной жизни и восстановления трудоспособности. Таким образом, через 3 месяца после операции наблюдалось 84 % отличных и хороших результатов лечения и 16 % удовлетворительных. А через год после операции 93 % отличных и хороших результатов при 7 % удовлетворительных.
У 4 больных первоначальный результат ППЛДД был недостаточным и поэтому была произведена повторная ППЛДД; после чего у 3 больных достигнут отличный и хороший результат, а у одного удовлетворительный.
Открытая нуклеотомия произведена у двух пролеченных методом ППЛДД больных в других клиниках по их настоянию без убедительных показаний.
Осложнения наблюдались у 4 больных, их которых у двух были кратковременные радикулопатии и в двух случаях была клиника асептического дисцита, что потребовало дополнительного противовоспалительного лечения в течение двух-трех недель.
В качестве иллюстрации результатов лечения можно рассмотреть несколько компьютерных томограмм поясничного отдела позвоночника до и после проведения ППЛДД.
Больная 43 лет , в течение нескольких лет боли в поясничном отделе позвоночника, синдром люмбоишиалгии. За 1,5 месяца до хирургического лечения боли значительно усилились. Больная не могла сидеть и ходить. На компьютерных томограммах определяется грыжа диска в сегменте L 4 — L 5 парамедианная слева, перекрывающая более 50 % позвоночного канала, резко сдавливающая дуральный мешок и левый корешок L 5 . После выполнения ППЛДД наблюдался полный немедленный регресс болевого синдрома. Быстро восстановилась статика и биомеханика позвоночника. На контрольных компьютерных томограммах, выполненных через 3 месяца, отмечается полное рассасывание грыжевого выпячивания как на аксиальных срезах, так и при реконструкции в сагиттальной плоскости (рис. 3). Дуральный мешок расправлен, визуализируется левый пятый поясничный корешок.
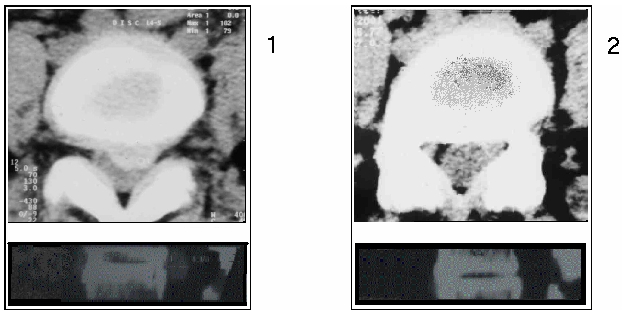 |
| Рис. 3. Компьютерные томограммы больной 43 лет: 1 – до операции; 2 – спустя 3 месяца после ППЛДД. |
Больная 49 лет , поясничный остеохондроз, парамедианная грыжа L 5 — S 1 , справа. Больную беспокоили сильные боли корешкового характера в покое и при движениях, ослабленное сгибание левой стопы. После выполнения ППЛДД регресс синдрома радикулоишемии S 1 справа в течение нескольких часов. В течение нескольких дней полное исчезновение болевого синдрома. На контрольных компьютерных томограммах отмечается почти полное рассасывание грыжи диска, дуральный мешок расправлен (рис. 4).
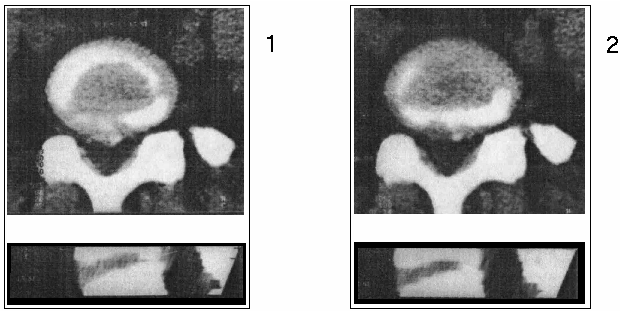 |
| Рис. 4. Компьютерные томограммы больной 49 лет: 1 – до операции; 2 – спустя 3 месяца после ППЛДД. |
Обсуждение
Предложенный нами метод (ППЛДД) для лечения больных с рефлекторно-компрессионными синдромами поясничного остеохондроза обладает широким диапазоном действия и может применяться как на стадии люмбалгий с профилактической целью, так и при более серьезной патологической ситуации. В частности, хорошие результаты, полученные при лечении радикулоишемий можно объяснить не только декомпремирующим воздействием, но и влиянием лазерной энергии на микроциркуляцию. Мы также не заметили большой зависимости результатов лечения от величины грыжевого выпячивания. Более того, почти во всех таких случаях получен отличный и хороший результат. По нашим наблюдениям больше проблем создают задне-боковые грыжи диска небольших размеров, но плотной консистенции.
Хорошие и относительно быстрые результаты лечения после применения ППЛДД можно объяснить тем, что данный метод, впрочем как и другие способы неэндоскопической лазерной хирургии дисков, является принципиально новым технологическим приемом и стоит на порядок выше любой механической дискэктомии, поскольку использует многофакторное энергетическое воздействие на все структуры позвоночника и позвоночного канала.
Кроме значительного падения давления в диске при ППЛДД с применением аппарата «Лазон-10-П» происходит интенсивная вапоризация, так как применяемая длина волны в 960 нм активно поглощается молекулами воды. Во время прохождения лазерной энергии в хрящевой ткани развиваются процессы тепло- и массопереноса вследствие перехода связанной воды в свободную. Протогликаны матрикса хряща приобретают подвижность, приводящую к релаксации напряжений или денатурации белковых молекул [12]. Денатурация белка в зоне лазерного излучения и уменьшение содержания воды сразу за этой зоной приводит к сжатию диска, которое продолжается и после отключения лазера [9].
Заключение
Таким образом, метод ППЛДД с использованием полупроводникового аппарата «Лазон-10-П» обнаруживает высокую эффективность, запуская механизм ускоренной инволюции грыжевых выпячиваний вследствие интенсивной вапоризации, выраженной декомпрессии и денатурации диска.
Он имеет мало противопоказаний, к которым можно отнести свободный или секвестральный фрагмент диска, выраженные проявления спондилеза и спондилоартроза, а также спондилолистез больше I степени.
Преимуществами метода являются местная анестезия, минимальная инвазивность, отсутствие процессов рубцевания в эпидуральном пространстве, короткий период недееспособности (4-6 недель).
Большое значение имеет возможность повторения процедуры, отсутствие противопоказаний для мануальной терапии и возможной последующей открытой операции. Следует также отметить высокую технологичность и экономичность метода ППЛДД.
Список литературы
-
Антонов И.П. Заболевания нервной системы. Минск. 1992г.
-
Антонов И.П. Классификация заболеваний периферийной нервной системы и формулировка диагноза. Журнал невропат. и психиатрии. 1985, № 4, с. 481-487.
-
Ветрилэ С.Т., Погожева Е.И., Стеблин Н.И. Тактика лечения больных остеохондрозом позвоночника с применением папаина. Остеохондроз позвоночника (Мат.Ер. сов-амер. симпозиум) М., 1992, с 142-147.
-
Казьмин А.И., Ветрилэ С.Г., Джалилов Я.Р. Оперативное лечение поясничного остеохондроза. Ортопед. травматол. 1986. № 10, с. 17-20.
-
Миронов С.П., Назаренко Л.М., Черкашов А.М., Бурлакова Т.М. Лечение остеохондроза поясничного отдела позвоночника методом лазерной дискэктомии. Вестник травматологии и ортопедии им. Н.Н. Приорова, 1999, № 2, 19-23.
-
Мовшович И.А. О нарушении стабильности позвоночника после расширенной ляминэктомии. Ортопед. травматол. 1970, № 6, с. 44-49.
-
Мовшович И.А., Шотемер Ш.Ш. К вопросу о нестабильности позвоночника Ортопед. травматол. 1979, № 5, с. 24-29.
-
Мусалатов Х.А., Аганесов А.Г. Хирургическая реабилитация корешкового синдрома при остеохондрозе поясничного отдела позвоночника. М. Медицина, 1998. с. 83.
-
Николаев А.П., Лазарев А.Ф., Смирнов И.И. Метод лазерной декомпрессии в лечении дискогенных поражений позвоночника. Кремлевская медицина № 1, 1999, 5-6.
-
Осна А.И. Основные принципы и задачи пункционного лечения остеохондроза позвоночника. В сб. научн. тр. Остеохондроз позвоночника (пункционное лечение). Л., 1975, с. 3-9.
-
Попелянский Я.Ю. Вертеброгенные заболевания нервной системы. Руководство. Йошкар-Ола: Мар. кн. изд-во, 1983, т. 2.
-
Соболь Э.Н., Китай М.С. Расчет кинетики нагрева и структурных изменений в хрящевой ткани под действием лазерного излучения. Квант. Электрон (Москва). 1998. 25, № 7, с. 651-654.
-
Хвисюк Н.И., Чикунов А.С. и др. патогенетические аспекты клиники и лечения остеохондроза позвоночника. В кн.: Остеохондроз позвоночника (Матер. сов.- амер. симпозиума) М., 1992, с. 3-9.
-
Цивьян Я.М. Хирургия позвоночника. М. Медицина. 1966. с. 312.
-
Шустин В.А., Панюшкин А.И. Клиника и хирургическое лечение дискогенных пояснично-кресцовых радикуломиелоишемий. Л., Медицина, 1985, с. 173.
-
Юмашев Т.С., Елизаров М.Н. и др. Наш опыт оперативного лечения остеохондроза позвоночника. Ортопед. травматол. 1984, № 8 с1-6.
-
Юмашев Т.С., Фурман М.Е. Остеохондрозы позвоночника, 1985г.
-
Юмашев Т.С., Фурман М.Е. Остеохондрозы позвоночника. М. Медицина. 1984. c. 382.
-
Ascher P., Holzer P., Sutter B. et al. Laser denaturation of nucleus pulposus of herniated intervertebral discs. In: Arthroscopie microdiscectomy 1991. P. 137-140.
-
Baruch S.K. Lancinating pain i post laminectomy chronic sciatica. Acta neurochir. 1985. Vol.76. № 3-4. P. 129-130.
-
Blanc C., Meyer A. et at. Treatment of herniated lumbar disc by percutaneous nucleotomy with aspiration. S. of Neuroradial. 1990. Vol. 17, № 3, P. 182-190.
-
Bouillet R. Complications de la nucleolyse discale par le Chymopapaine Acta orthopaed belg, 1987, 53, № 2, 250-260.
-
Caspar W. A new surgical procedure for lumbar disc herniation causing less tissue damage through a microsurgical approach. Adv. Neurosurg , 1997, № 4, P. 74-77,
-
Chiu S., Clifford T., Greenspan M., et al. Microdecompressive Percutaneous Endoscopy: Spinal Discectomy with new Laser Thermodiscoplasty for Non-Extruded Herniated Nucleus Pulposus. Surgical Technology International, Vol. № 14, pages 343-351.
-
Choy D.S. Percutaneous laser disc decompression (PLDD): twelve years experience with 752 procedures in 518 patients S Clin Laser Med Surg 1998 Dee; 16 (6): 325-3.
-
Choy D.S., Case R.B., Ascher P.N.: Percutaneous Laser ablation of lumbar disc. 33 red. Ann. Meeting Orthop. Research Soc. 1 (1987) 19.
-
Choy D.S., Case R.B., Fielding N., Hughes S., Liebet N., Ascher P. Percutaneous laser nucleolysis of lumbar disks. New England Southal of Medicine, 1987, Sep. 17, 317 (12), 771-2.
-
Choy D.S., Ngeas S. Percutaneous laser disc decompression in spinal stenosis. S. Clin. Laser. Med.Surg., 1998. Apr: 16 (2): 123-5.
-
Fontanella A. Combined Non-invasive. Technique in Herniated Lumbar Discs of Large Size: Chemonucleolysis and Percuneous Treatment Under Endoscope Control. Sixth Annual Meeting. USA , Arizona , March 10-13 , 1993 .
-
Kumbin P. Laser Nuclear ablation In: Arthroscopic microdiscectomy. Baltimore . USA . 1991. P. 133-136.
-
Martin H. Savitz, Havatal Donghty R.N. and Paul Burks. Percutaneous lumbar discectomy with a working endoscopy and laser assistance. Neurosurg. Focus 4 (2): Article 3, 1998.
-
Mc Cullogh S. Complication of lumbar microdiscectomy. Acta orthopaed. belg. 1987 , 53, № 2, с. 272-275.
-
Nijikata S. Percutaneous Nucleotomy – a new concept technical and 12 years experience Clin orthorp. 289: 9-23, 1989.
-
Oldenkoff P., Roost D. Treatment microchirurgical de la hernia discale lombair. Neurochirurgical (Paris), 1980? 26 . № 3, с. 234-299.
-
Onik G. Matoon S.C., Davis G.N. Automated percutaneous discectomy: et prospective multi institutional study. Neurosurgery 2:228, 1990.
-
Quigley M.R., Shin T., Elrilai A. et al. Percutaneous discectomy with the Ho: GAG Laser. Laser in Surgery and Indierne. 1992, 12 (6); 621-4.
-
Schaffer S., Kambin P. Percutaneous posterolateral lumbar discectomy and decompression with a 6,9 millimeter cannula, S, Bone Joint Surg Am. 73. 322-831, 1991.

